Søknad om vesentlig endring i klinisk studie av legemiddel til mennesker
Publisert:
|
Oppdatert:
Endringer
- : Mindre rettelser for å forbedre innholdet
Innhold på siden
Hva er en vesentlig endring?
Etter at en klinisk studie er godkjent under forordningen, kan sponsor gjøre følgende endringer av studiedokumentasjonen:
- Vesentlige endringer (CTR art 2.2.13): Søknad om vesentlig endring innsendes i Clinical Trials Information System (CTIS).
- Endringer som ikke er vesentlige, men som er relevante for medlemslandenes mulighet for å overvåke studien (CTR art 81.9): Sponsor skal oppdatere relevant informasjon i CTIS.
- Ikke-vesentlige endringer (endringer som ikke vurderes som vesentlige og som ikke er relevante for medlemslandenes mulighet for å overvåke studien): Krever ikke søknad i CTIS.
En endring anses for vesentlig dersom:
-
Endringen kan ha en vesentlig påvirkning på forsøkspersonenes sikkerhet, helse eller rettigheter.
-
Endringen kan ha en vesentlig påvirkning på robustheten eller påliteligheten til de dataene som genereres i forbindelse med utprøvingen.
Definisjon på vesentlig endring i forordningen:
“Any change to any aspect of the clinical trial which is made after notification of a decision referred to in Articles 8, 14, 19, 20 or 23 of the CTR and which is likely to have a substantial impact on the safety or rights of the subjects or on the reliability and robustness of the data generated in the clinical trial"
Det er sponsors ansvar å vurdere om en endring er vesentlig. Eksempler på vesentlige og ikke-vesentlige endringer finnes i Regulation (EU) No 536/2014 Questions & Answers, Annex IV.
Søknaden
For informasjon om hvordan søknaden opprettes i CTIS, se CTIS Sponsor Handbook, kapittel 4.3 Chapter III Authorisation procedure for a substantial modification of a clinical trial.
En søknad om vesentlig endring kan gjelde del I, del II eller både del I og del II.
Tekniske begrensninger i CTIS tillater kun saksbehandling av én søknad om gangen. Dette betyr at en søknad om vesentlig endring på del I ikke kan sendes inn i CTIS så lenge det er pågående saksbehandling som gjelder del I.
Godkjenningsprosedyren for vesentlige endringer er beskrevet i CTR, Chapter III Authorisation procedure for a substantial modification of a clinical trial.
En sjekkliste for hvilken dokumentasjon som skal vedlegges søknaden og som skal sendes inn via CTIS finnes i CTR, Annex II Application Dossier for Substantial Modification .
Følgebrev og endringsbeskrivelse
Ved søknad om vesentlig endring skal et følgebrev og en beskrivelse av de aktuelle endringene vedlegges søknaden.
For informasjon om hvilke opplysninger som skal inkluderes i følgebrevet og endringsbeskrivelsen, se CTR, Annex II.
Vi anbefaler å bruke malene «Cover letter» og «Modification description» som kan lastes ned fra nettsiden Clinical Trials Coordination Group (CTCG), Key document list.
Dersom endringen medfører forandringer i opprinnelig innsendte strukturerte data i CTIS så må dette oppdateres.
Dokumentasjon
Endrede dokumenter eller utdrag av dokumenter, med oppdatert versjonsnummer og dato, skal sendes inn både i en versjon som viser den tidligere og den nye ordlyden som sporede endringer, og i en ren versjon som kun viser den nye ordlyden. Dersom endringene i et dokument er mange og utspredt skal endringene oppsummeres.
Alle endrede dokumenter må oppdateres med korrekt dato og versjonsnummer.
Hvis søknaden om vesentlig endring krever endringer i informasjonen i skjemaet i CTIS, skal skjemaet oppdateres samtidig med innsendingen.
Hvis aktuelt skal søknaden kompletteres med for eksempel en oppsummering av data, oppdatert versjon av nytte/risiko og konsekvenser for forsøkspersoner som allerede er inkludert i utprøvingen. Se Regulation (EU) No 536/2014, Annex II, del E "Supporting information".
Hvis aktuelt skal søknaden kompletteres med for eksempel en oppsummering av data, oppdatert versjon av nytte/risiko og konsekvenser for forsøkspersoner som allerede er inkludert i utprøvingen.
Se Regulation (EU) No 536/2014, Annex II, del E "Supporting information".
Tidslinje
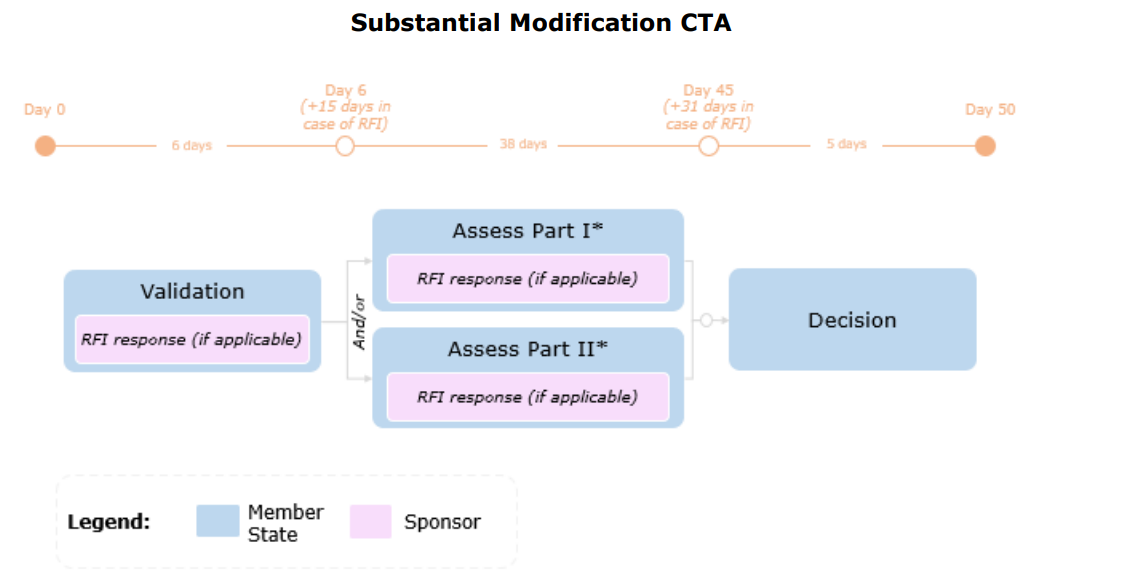
Endringer i henhold til Artikkel 81.9
Strukturerte data i CTIS og/eller relevante dokumenter skal oppdateres av sponsor dersom det gjøres endringer som ikke er vesentlige endringer, men som er relevante for medlemslandenes overvåkning av studien.
CTR Article 81.9: The sponsor shall permanently update in the EU database information on any changes to the clinical trials which are not substantial modifications but are relevant for the supervision of the clinical trial by the Member States concerned.
Ikke-vesentlige endringer
Ikke-vesentlige endringer er endringer som ikke vurderes som vesentlige og ikke er relevante for medlemslandenes mulighet for å overvåke studien. Disse endringene krever ikke søknad i CTIS.
Følgebrevet ved neste søknad om vesentlig endring skal inneholde en oversikt over alle ikke-vesentlige endringer som er gjort siden forrige godkjenning
Ikke-vesentlige endringer skal dokumenteres fortløpende i Trial Master File.
For mer informasjon om ikke-vesentlige endringer, se Regulation (EU) No 536/2014 Questions & Answers, Section 3.4.
Gebyr
Fakturainformasjon skal oppgis i del I (Proof of payment) av søknaden i CTIS. Det blir sendt faktura etter at søknad er mottatt. Fakturaen vil påføres EU CT nummer og DMPs saksnummer.
Klikk her for informasjon om gebyrer for kliniske utprøvinger av legemidler.
Relevante lenker
-
QUESTIONS & ANSWERS, Clinical Trials Regulation (EU) No 536/2014, chapter 3
-
Oversikt over nasjonale krav til del 2 finnes på REK-portalen.
- CTIS Sponsor Handbook (pdf)
- Heads of Medicines Agencies: Clinical Trials Coordination Group (CTCG)