Klassifisering av medisinsk utstyr
Publisert:
|
Oppdatert:
Endringer
Medisinsk utstyr deles inn i risikoklasser, basert på risikoen forbundet med bruk. Klassifisering innebærer å avgjøre utstyrets risikoklasse. Produsenten er ansvarlig for å klassifisere utstyret sitt, basert på utstyrets tiltenkte formål.
Medisinsk utstyr deles inn i 4 risikoklasser som spenner fra lav til høy risiko: klasse I, IIa, IIb og III. Produsentens tiltenkte formål og mulig risiko forbundet med bruk avgjør risikoklassen.
IVD-utstyr deles også inn i 4 risikoklasser som spenner fra lav til høy risiko: klasse A, B, C og D. Som for medisinsk utstyr, avgjøres risikoklassen av produsentens tiltenkte formål og mulig risiko ved bruk av produktet. For IVD-utstyr omfatter risikoen ved bruk av produktet både risikoen for det enkelte individ, og risikoen for folkehelsen.
Prinsipper ved risikoklassifisering
Risikoklassen bestemmes ved at produsenten sammenligner tiltenkt formål opp mot et sett klassifiseringsregler. Tiltenkt formål er definert i MDR artikkel 2 (12) som " den bruken som et utstyr er beregnet på ifølge produsentens opplysninger i merkingen, i bruksanvisningen eller i markedsførings- eller salgsmateriale eller -uttalelser, og som er angitt av produsenten i den kliniske evalueringen". Tilsvarende definisjon finnes i IVDR artikkel 2 (12).
For medisinsk utstyr finnes klassifiseringsreglene i MDR vedlegg VIII, og for IVD-utstyr, i IVDR vedlegg VIII.
Nedenfor er noen punkter å ha i bakhodet ved bruk av reglene for bestemmelse av risikoklasse:
-
Det er produsenten som er ansvarlig for å klassifisere sitt eget produkt.
-
Det er produsentens tiltenkte formål med utstyret, og ikke utilsiktede formål (f.eks. bruk utenfor angitt bruksområde), som avgjør hvilken klasse utstyret tilhører.
-
Medisinsk utstyr ment for bruk sammen med annet utstyr klassifiseres for seg.
-
Tilbehør til medisinsk utstyr skal klassifiseres for seg og atskilt fra utstyret det brukes sammen med.
-
Programvare som styrer utstyr eller påvirker bruken av utstyr, skal tilhøre samme klasse som utstyret.
-
Programvare som er uavhengig av annet utstyr, skal klassifiseres for seg.
-
Dersom utstyret er beregnet på flere bruksområder skal det klassifiseres på grunnlag av den bruken som er mest risikofylt.
-
Hvis utstyret kan klassifiseres i henhold til flere regler, er det regelen som gir høyes risikoklasse som gjelder.
Risikoklassifisering av medisinsk utstyr
Medisinsk utstyr deles inn i 4 risikoklasser som spenner fra lav til høy risiko: klasse I, IIa, IIb og III. Risikoklassen avgjøres av produsentens tiltenkte formål og mulig risiko forbundet med bruk av utstyret.
Figuren nedenfor illustrerer sammenhengen mellom risikoklasse, risiko, og krav om involvering av meldt organ.
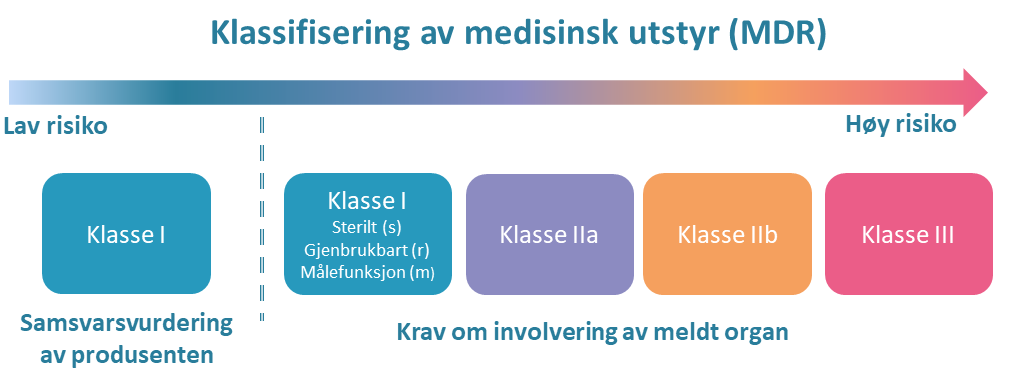
-
Klasse I (Is, Im og Ir): Lav risiko forbundet med bruk. For utstyr i klasse I som bringes i omsetning i steril tilstand (Is), har en målefunksjon (Im) eller som er gjenbrukbart kirurgisk utstyr (Ir), må meldt organ involveres for samsvarsvurdering av de delene som angår sterilisering, målefunksjon og gjenbruk.
-
Klasse IIa: Moderat risiko forbundet med bruk. Krever samsvarsvurdering av meldt organ.
-
Klasse IIb: Moderat til høy risiko forbundet med bruk. Krever samsvarsvurdering av meldt organ.
-
Klasse III: Høy risiko forbundet med bruk. Krever samsvarsvurdering av meldt organ.
Risikoklassen bestemmes ved at produsenten sammenligner utstyrets tiltenkte formål opp mot 22 klassifiseringsregler som finnes i MDR vedlegg VIII. DMP har utarbeidet en oversikt over klassifiseringsreglene i MDR på norsk, som kan lastes ned.
MDR - Oversikt klassifiseringsregler (pdf)
EU-kommisjonen har utarbeidet en veileder med eksempler på klassifisering av medisinsk utstyr, MDCG 2021-24 (se vår oversikt over nyttige lenker nederst på siden).
Risikoklassifisering av IVD-utstyr
IVD-utstyr deles inn i 4 risikoklasser som spenner fra lav til høy risiko: klasse A, B, C og D. Som for medisinsk utstyr avgjøres risikoklassen av produsentens tiltenkte formål og mulig risiko forbundet med bruk av utstyret. For IVD-utstyr omfatter risikoen ved bruk av utstyret både risikoen for det enkelte individ, og risikoen for folkehelsen.
Figuren nedenfor illustrerer sammenhengen mellom risikoklasse, risiko, og krav om involvering av meldt organ:
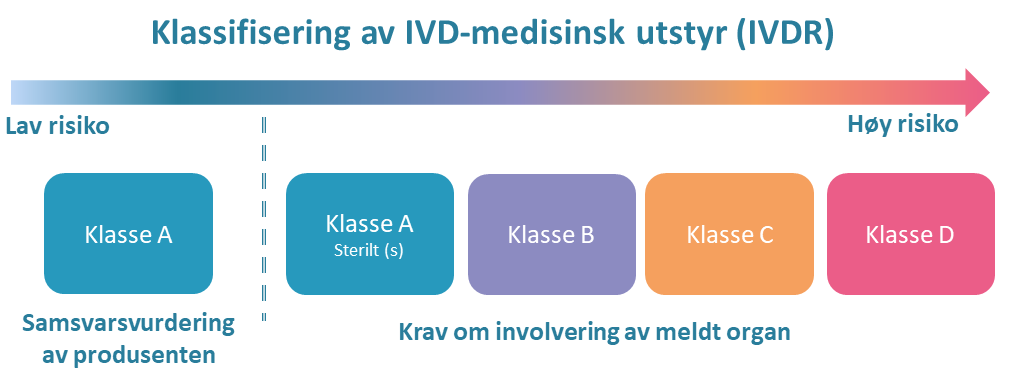
-
Klasse A: Lav individuell risiko og lav risiko for folkehelsen. For utstyr i klasse A som bringes i omsetning i steril tilstand, må meldt organ involveres for samsvarsvurdering av de delene som angår sterilisering.
-
Klasse B: Moderat individuell risiko og/eller lav risiko for folkehelsen. Krever samsvarsvurdering av meldt organ.
-
Klasse C: Høy individuell risiko og/eller moderat risiko for folkehelsen. Krever samsvarsvurdering av meldt organ.
-
Klasse D: Høy individuell risiko og høy risiko for folkehelsen. Krever samsvarsvurdering av meldt organ.
EU-kommisjonen har utarbeidet en veileder med eksempler på klassifisering av IVD-utstyr, MDCG 2020-16 (se vår oversikt over nyttige lenker nederst på siden).
Hvilken betydning har risikoklassen
Risikoklasse er avgjørende for hvilken prosedyre som skal benyttes før markedsplassering, også kalt samsvarsvurdering. Risikoklassen vil blant annet avgjøre om utstyret skal vurderes og følges opp av et meldt organ.
Nyttige EU-veiledere for kvalifisering og klassifisering
- MDCG 2021-24 Veileder for klassifisering av medisinsk utstyr
- MDCG 2024-11 Veileder for kvalifisering av IVD-utstyr
- MDCG 2020-16 Veileder for klassifisering av IVD-utstyr
- MDCG 2019-11 Kvalifisering og klassifisering av software under MDR og IVDR
- Flytskjema for kvalifisering av software som medisinsk utstyr