Trinnpris - ikke-patenterte legemidler
Publisert:
|
Oppdatert:
Endringer
- : Juster plassering på noen avsnitt.
Når et legemiddel mister sin patentbeskyttelse, kan det komme konkurranse fra andre som produserer likeverdige legemidler med det samme virksomme stoffet som det opprinnelige legemiddelet.
Innhold på siden
Trinnpris kan tre i kraft straks det lanseres en generisk eller biotilsvarende konkurrent til en originalmedisin, og DMP har vurdert at medisinene er likeverdige og kan byttes i apotek. Ordningen gjelder for medisiner både på hvit og blå resept.
Legemidler som finansieres av helseforetakene er unntatt trinnprisregulering.
Hva er trinnpris?
Trinnprissystemet ble innført i 2005 for å redusere Folketrygdens og pasientenes legemiddelkostnader. I trinnprissystemet reduseres prisen på et legemiddel trinnvis med faste kuttsatser etter at legemiddelet har mistet patentbeskyttelse, fått konkurranse fra likeverdige legemidler og kommet på DMPs liste over byttbare legemidler.
Hvorfor trinnpris?
Når patentet løper ut og originallegemidlene får konkurranse av generiske eller biotilsvarende preparater, forhandler grossistene om lavere priser fra legemiddelfirmaene. Grossistene får ofte senket prisen på originallegemiddelet, i tillegg til at likeverdige legemidler introduseres til en lavere pris.
Trinnprissystemet er en enkel måte myndighetene kan sikre at også folketrygd og pasient kan nyte godt av lavere legemiddelpriser.
Folketrygd og pasient sparer tilsammen over 2,5 milliarder kroner årlig på trinnpris og medisin bytte. Medisinbytte og trinnpris betyr altså at både myndighetene og pasientene kan få plass til andre viktige tiltak på sitt budsjett uten at det medisinske tilbudet svekkes.
Trinnprismodellen
Trinnprismodellen er en regulering av AUP (apotekets utsalgspris). Likevel fastsetter vi trinnprisen ved prosentvise kutt i originallegemiddelets maksimale AIP (apotekets innkjøpspris) da første generika eller biotilsvarende legemiddel fikk fastsatt maksimalpris. Etter at AIP er kuttet, legges apotekavanse og 25 % merverdiavgift til.
Kuttsatsene avhenger av omsetningen av virkestoffet før generisk eller biotilsvarende konkurranse inntraff var under eller over 100 millioner kroner. Virkestoffene med omsetning på over 100 millioner kroner får de største kuttene. Kuttsatsene er forskjellige for syntetiske og biologiske legemidler, hvor biologiske legemidler får fastsatt noe lavere kuttsatser.
Prisene reduseres som vist i figurene under. I tillegg til hovedmodellen, som fremgår av figuren, har virkestoffene atorvastatin, simvastatin og pantoprazol et kutt på henholdsvis 94, 96 og 88 prosent.
For virkestoff som fortsatt omsetter for mer enn 100 mill kroner etter første trinnpriskutt, vil det gjelde et kutt på 90 %.
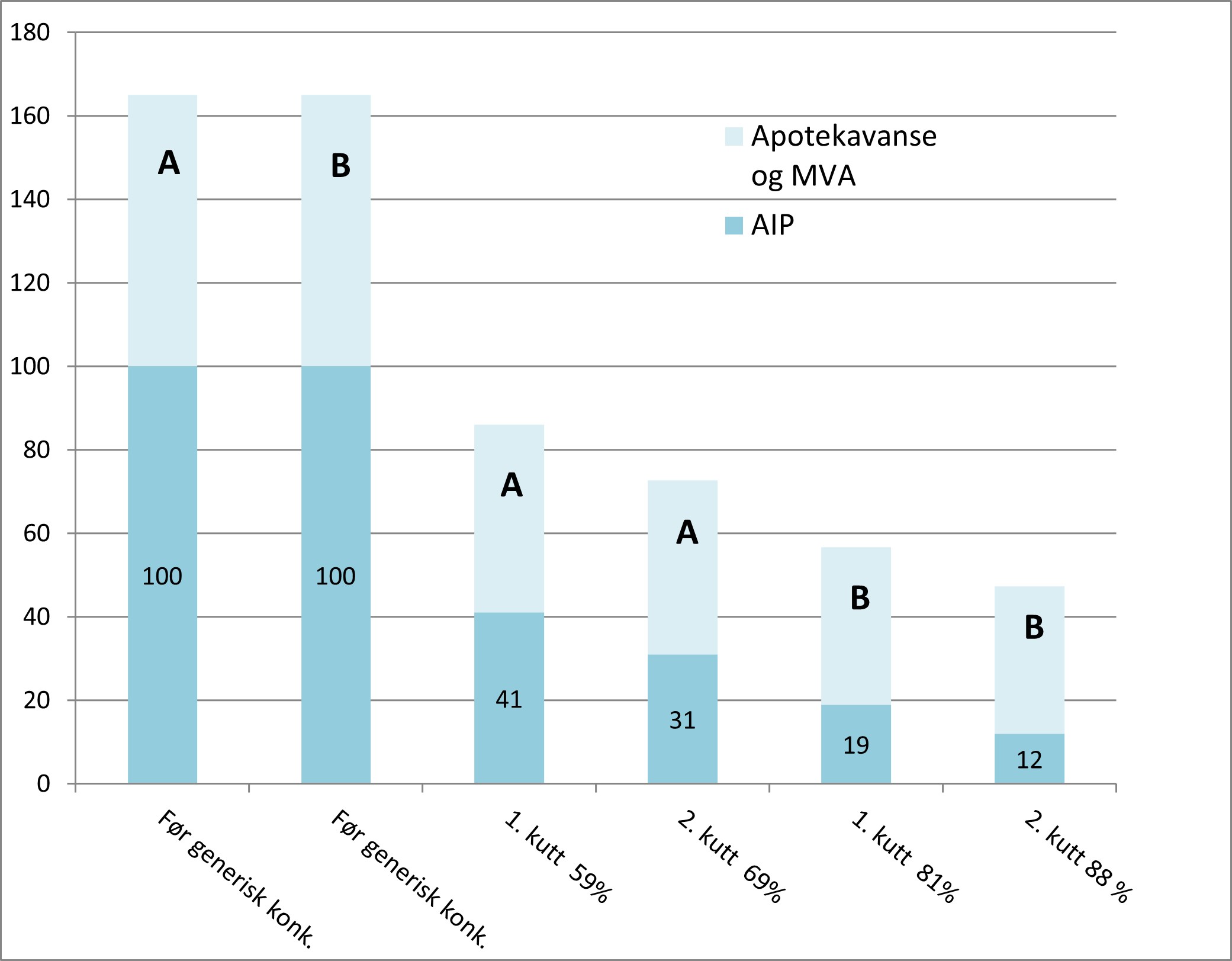
Syntetiske legemidler
AIP kuttes i et til to trinn. Det første trinnet inntrer ved generisk konkurranse. Det andre kuttet kommer tidligst 18 måneder etter det første trinnet.
| Omsetning før generisk konkurranse |
1. trinnpriskutt (umiddelbart) |
2. trinnpriskutt (tidligst etter 18 måneder) |
| Under 100 mill. kroner | 59 % | Omsetning > 15 mill. kroner: 69% |
| Over 100 mill. kroner | 81 % |
Omsetning > 30 mill. kroner: 88% Omsetning > 100 mill. kroner: 90% |
Syntetiske legemidler
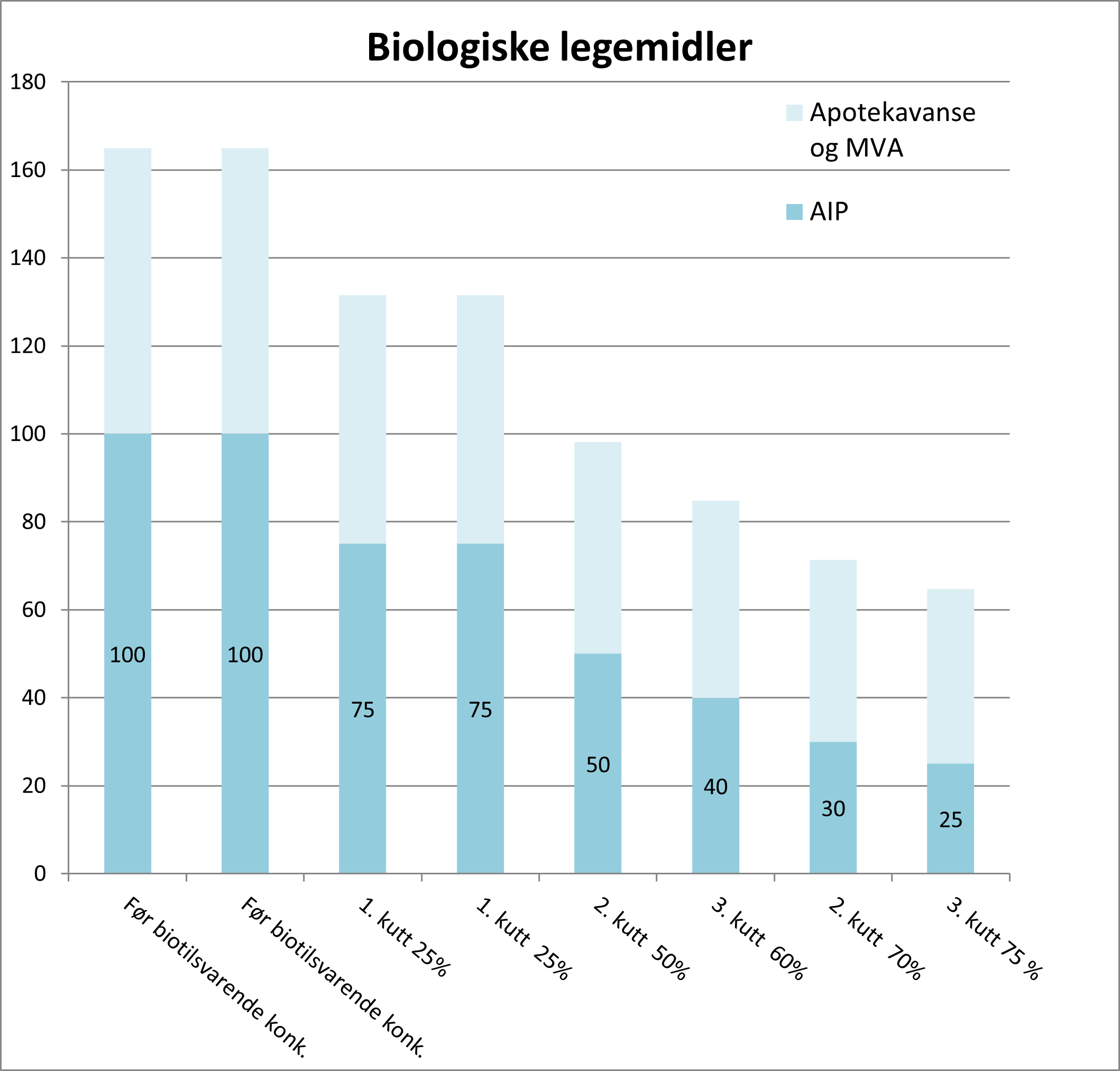
Biologiske legemidler
AIP kuttes i to til tre trinn. Det første trinnet inntrer ved biotilsvarende konkurranse, mens det andre trinnet kommer 6 måneder senere. Det tredje kuttet kommer tidligst 12 måneder etter det andre trinnet.
| Omsetning før biotilsvarende konkurranse | 1. trinnpriskutt (umiddelbart) |
2. trinnpriskutt (etter 6 mnd) |
3. trinnpriskutt (tidligst etter 18 måneder) |
| Under 100 mill. kroner | 25 % | 50 % | Omsetning > 15 mill. kroner: 60% |
| Over 100 mill. kroner | 25 % | 70 % |
Omsetning > 30 mill. kroner: 75% Omsetning > 100 mill. kroner: 80% |
Rutiner ved inkludering av nye virkestoff i trinnprissystemet
Legemiddelforskriftens § 12-14, 2. og 3. ledd:
«Felles trinnpris for legemidler i en byttegruppe fastsettes etter § 12-15 når:
- legemidlene er oppført på DMPs bytteliste, jf. lov 2. juni 2000 nr. 39 om apotek § 6-6 og forskrift 27. april 1998 nr. 455 om rekvirering og utlevering av legemidler fra apotek § 8-7 og,
- originalpreparatet har stabil generisk eller biotilsvarende konkurranse i Norge fra minst ett legemiddel.
Stabil generisk eller biotilsvarende konkurranse anses å foreligge når legemidlene er oppført på byttelisten og det ikke kan dokumenteres alvorlige leveringsproblemer for det generiske eller biotilsvarende legemiddelet.»
Rutiner ved inklusjon av nye virkestoff i trinnprissystemet
Før legemidler føres på byttelisten, har firmaene søkt om og fått markedsføringstillatelse, samt maksimalpris.
Etter at legemidler med nye virkestoff blir oppført på byttelisten, kan DMP legge til grunn at det er konkurranse, såfremt det ikke er dokumentert alvorlige leveringsproblemer for det generiske eller biotilsvarende legemiddelet.
Før vi varsler om inklusjon i trinnprissystemet, pleier DMP likevel å undersøke nærmere situasjonen for salg av generika eller biotilsvarende i Norge. I hovedsak gjør vi det på to ulike måter:
- Ved å konstatere at det faktisk har vært salg av generika eller biotilsvarende i Norge
- Ved å innhente en bekreftelse fra MT-innehaver av det generiske eller biotilsvarende legemiddelet på at disse er leveringsdyktige.
Konstatere at det faktisk har vært salg av generika eller biotilsvarende i Norge
DMP sjekker salgsstatistikken fra Farmalog og registrerer om det er salg av generika eller biotilsvarende.
Generika eller biotilsvarende leverandør bekrefter at han er leveringsdyktig
Det har vært mange tilfeller hvor generikaleverandører faktisk er på markedet og tilbyr preparatene til grossistene, men hvor grossistene likevel har valgt å inngå avtale med originalleverandør. Da blir det ikke noe salg av generika, selv om originalpreparatet er utsatt for generisk konkurranse.
Ifølge forskriften er det tilstrekkelig at generika eller biotilsvarende har kommet på byttelisten, og at det ikke er dokumentert alvorlige leveringsproblemer for at trinnpris kan innføres. DMP har imidlertid pleid å undersøke hos leverandør om firmaet er leveringsdyktig og fra hvilket tidspunkt de var/blir leveringsdyktige. Dersom vi får en slik skriftlig bekreftelse, går vi ut fra at forskriftens krav til stabil generisk konkurranse i alle fall er oppfylt fra tidspunktet leverandøren oppgir. Vi går så videre med å varsle inklusjon i trinnprissystemet.
I tilfeller der generika eller biotilsvarende leverandøren ved rettslig kjennelse har blitt ilagt forbud mot å omsette det aktuelle virkestoffet, vil dette regnes som et alvorlig leveringsproblem. Denne perioden vil bli trukket fra ved beregning av når trinnpriskuttene inntreffer.
Vi anser innmeldingen til Farmalogg som et teknisk spørsmål, men som bør være i orden av praktiske årsaker. Det er ikke avgjørende for å fastslå at det er stabil generisk konkurranse.
Skjønnsmessig beregnet trinnpris
DMP har ifølge legemiddelforskriftens § 12-15, 11. ledd, hjemmel til å fastsette en skjønnsmessig beregnet trinnpris dersom beregningen av trinnpris gir en urimelig lav pris. Bruk av de vanlige satsene kan noen ganger gi så lave priser at det ikke vil være lønnsomt for leverandører av generika eller biotilsvarende å selge. DMP etablerer i disse tilfellene en dialog med leverandører av generika eller biotilsvarende for å finne fram til satser som gjør at leverandørene kan bekrefte at de er leveringsdyktige.
Forhåndsvarsel, orientering til aktørene og vedtak
Inklusjon av nye virkestoff i trinnprissystemet, skjer på følgende måte:
- Legemiddelleverandørene (både original, PI, generika og biotilsvarende) varsles ved e-post. De får som regel 14 dagers frist til å uttale seg.
- Apotekforeningen, LMI, Farma Norge, grossistene og HOD blir satt opp som kopimottakere. Dersom disse vil uttale seg, oppfordres de til å gjøre det innen samme frist som leverandørene fikk.
- Uttalelser kommer inn – per e-post
- DMP vurderer uttalelsene og fatter deretter vedtak som sendes til de samme som fikk varselet tilsendt.
Patentstridigheter
Det er en grunnleggende forutsetning for generisk eller biotilsvarende konkurranse at patentet utløper. Trinnpris kan innføres uavhengig av pågående rettsstridigheter. Men DMP tar hensyn til rettskraftige avgjørelser.
Oversikt over trinnpriser og virkestoff inkludert i trinnprissystemet
- Oversikt over virkestoff inkludert i trinnprissystemet (per 17.02.2026 excel)
- Oversikt over pakninger med trinnpris (per 01.04.2026 excel)
Hva betyr trinnpris for legene?
Legene må forholde seg til at det kommer nye likeverdige legemidler på markedet. De må vurdere om det er tungtveiende medisinsk grunner som taler mot at apoteket kan tilby bytte av forskrevet medisin med det apoteket har til trinnpris. En slik grunn kan være at det er betydelig risiko for at pasienten ikke klarer å holde orden på medisinene sine etter bytte, og derfor bruker dem feil. Leger kan ikke vite hvilke apotek som har hvilke legemidler til trinnpris, og skal bare reservere mot bytte av medisinske grunner. Dette gjelder også om man skriver ut ett bestemt generika eller biotilsvarende merke. Det er nemlig ikke sikkert apoteket har det forskrevne merket til trinnpris. Da vil reservasjon fra lege føre til at pasienten får det forskrevne legemiddelet til maksimalpris, og folketrygden må betale mellomlegget mellom maksimalpris og trinnpris.
Forskrivning av virkestoff kan være en god løsning for mange pasienter.
Hva betyr trinnpris for pasienten?
Pasienter som ikke bytter til rimeligere medisin når apoteket tilbyr det, må selv betale mellomlegget mellom trinnpris og maksimalpris. Dersom legen reserverer mot bytte på blå resept, betaler folketrygden mellomlegget.
For hvite resepter er det alltid pasienten som betaler mellomlegget.
Dersom apoteket tilfeldigvis har det forskrevne legemiddelet til trinnpris, blir det ikke noe mellomlegg, verken for pasient eller folketrygd.
Tabellen nedenfor viser eksempler på mellomlegget mellom maksimalpris og trinnpris. Beløp er oppgitt i NOK pr november 2024.
| Pakning | Maksimalpris | Trinnpris | Mellomlegg |
| Tamsulosin og dutasterid 0,5mg/0,4mg, 90 kapsler | 680,40 | 326,80 | 353,60 |
| Sitagliptin 10 mg, 98 tabletter | 680,50 | 382,50 | 298,00 |
| Valsartan og amlodipin 5mg/160mg, 98 tabletter | 510,70 | 286,00 | 224,70 |
Hva betyr trinnpris for apotek og grossist?
Apotekene er pliktig å ha minst ett legemiddel til trinnpris innen hver byttegruppe. For disse medisinene vil apoteket tilby kunden å bytte forskrevet legemiddel med det legemiddelet apoteket har til trinnpris. Dersom et legemiddel leveres i både små og store pakninger, skal apotek kunne utlevere både liten og stor pakning til en utsalgspris lik trinnpris. Grossistene skal tilby apotekene legemidler som gjør dem i stand til å opprettholde disse forpliktelsene