Krav til importører og distributører
Publisert:
|
Oppdatert:
Endringer
Importør er den som bringer utstyr fra en tredjestat i omsetning innenfor EU. Distributør er den i omsetningskjeden, utenom produsenten eller importøren, som gjør utstyr tilgjengelig på markedet fram til ibruktaking.
Innhold på siden
Hvilke krav gjelder for importører og distributører
I tabellen nedenfor er noen av kravene til importører og distributører listet opp. Listen er ikke fullstendig. Krav og forpliktelser til produsenter finnes flere steder i MDR og IVDR og det er viktig at importører og distributører setter seg inn i alt av regelverket som er relevant for deres rolle som markedsaktør. Se også MDCG 2021-27 rev 1 Questions and Answers on Articles 13 & 14 of Regulation (EU) 2017/745 and Regulation (EU) 2017/746
| Artikkel | Oversikt over noen av kravene | Importør | Distributør |
|---|---|---|---|
|
MDR artikkel 10a IVDR artikkel 10a |
Videreformidle informasjon fra produsenten om forventet avbrudd i levering til neste ledd i forsyningskjeden. Det vil si andre markedsdeltagere, helseinstitusjoner og helsepersonell som de leverer utstyret direkte til. |
ü | ü |
|
MDR artikkel 13 og 14 IVDR artikkel 13 og 14 |
Generelle krav til kontroll av:
|
ü | |
Generelle krav til kontroll av:
|
ü | ü | |
Angi på utstyret, emballasjen eller dokumentasjonen som følger med:
|
ü | ||
Kontrollere at utstyret, emballasjen eller dokumentasjonen som følger med angir
|
ü | ||
Dersom utstyret ikke oppfyller regelverket:
|
ü | ü | |
| Påse at det føres register over klager og tilbaketrukket utstyr. | ü | ü | |
| Påse at informasjon om klager og tilbaketrukket utstyr videreformidles | ü | ü | |
| Sikre at det treffes nødvendige korrigerende tiltak | ü | ü | |
| Sikre korrekt lagring, oppbevaring og transport av utstyret | ü | ü | |
|
MDR artikkel 25 IVDR artikkel 22 |
Sørge for utstyrets sporbarhet i omsetningskjeden | ü | ü |
|
MDR artikkel 27 IVDR artikkel 24 |
Sørge for å lagre og oppbevare UDI-en for utstyr der dette er relevant | ü | ü |
|
MDR artikkel 30 IVDR artikkel 27 |
Påse at produsent og autorisert representant er blitt registrert innen to uker etter at utstyret er blitt gjort tilgjengelig på markedet | ü | |
|
MDR artikkel 31 IVDR artikkel 28 |
Registrering av importør | ü |
Oversikt over de ulike rollene for markedsdeltaker
| Markedsdeltaker | Definisjon i MDR artikkel 2 og IVDR artikkel 2 |
|---|---|
| Produsent | en fysisk eller juridisk person som framstiller eller helrenoverer utstyr, eller som får utstyr designet, framstilt eller helrenovert, og som markedsfører nevnte utstyr i eget navn eller under eget varemerke. |
| Autorisert representant | enhver fysisk eller juridisk person etablert i Unionen* som har fått og har akseptert en skriftlig fullmakt fra en produsent plassert utenfor Unionen, til å utføre bestemte oppgaver på dennes vegne med hensyn til dennes forpliktelser i henhold til denne forordning. |
| Importør | enhver fysisk eller juridisk person etablert i Unionen* som bringer utstyr fra en tredjestat i omsetning i Unionen*. |
| Distributør | enhver fysisk eller juridisk person i omsetningskjeden, utenom produsenten eller importøren, som gjør utstyr tilgjengelig på markedet fram til ibruktaking. |
| Helseinstitusjon | en organisasjon som har som hovedformål å pleie eller behandle pasienter eller fremme folkehelsen. |
* Med «Unionen» menes her EU/EØS-området og Tyrkia.
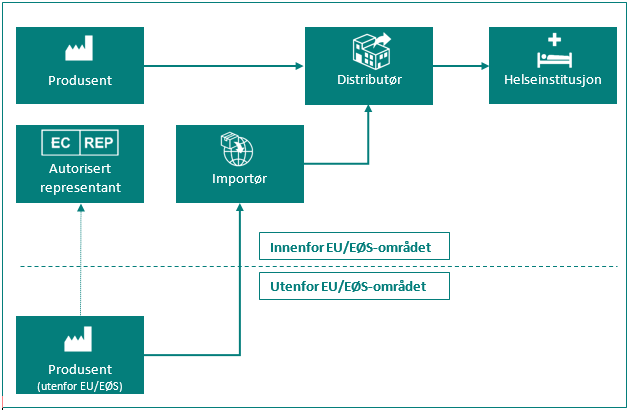
Figur: Markedsaktører i omsetningskjeden.