Krav til Helsevirksomheter
Publisert:
|
Oppdatert:
Endringer
Helseinstitusjon er en organisasjon som har som hovedformål å pleie eller behandle pasienter eller fremme folkehelsen.
Innhold på siden
Sporbarhet
Helseinstitusjoner skal, helst i elektronisk form, lagre og oppbevare UDI-koden for implanterbart medisinsk utstyr i klasse III som de har mottatt eller utlevert.
Det er viktig at helseinstitusjoner etablerer gode systemer og rutiner for sporbarhet av alle typer medisinsk utstyr for å få mest mulig ut av UDI-systemet.
For ytterligere detaljer se MDR artikkel 27 punkt 9.
«In-house» produsert medisinsk utstyr/unntaket
Regelverket tillater helseinstitusjoner å produsere, modifisere og bruke utstyr i egen virksomhet for å kunne møte en gitt pasientgruppes spesifikke behov, der hvor slikt behov ikke kan møtes tilfredsstillende med eksisterende produkter på markedet. Det stilles konkrete krav til egentilvirkning av slikt medisinsk utstyr.
For ytterligere detaljer se MDR artikkel 5 og IVDR artikkel 5
Les mer om in-house-produsert medisinsk utstyr.
Reprosessering av engangsutstyr
Virksomheter som reprosesserer medisinsk engangsutstyr vil være i å anse som produsent i henhold til MDR artikkel 17 punkt 2.
Fra og med 1. januar 2022 er reprosessering av medisinsk engangsutstyr ikke tillatt.
Gjennomføring av klinisk utprøving/ytelsesstudier
Helseinstitusjoner som selv sponser eller helsepersonell som deltar i en klinisk utprøving eller en ytelsesstudie, må være klar over sine forpliktelser.
For ytterligere detaljer se MDR artikkel 72 Gjennomføring av en klinisk utprøving og IVDR artikkel 68 Gjennomføring av en ytelsesstudie
Les mer om kliniske utprøvinger
Se og egen temaside for helsetjenesten
Forskrift om håndtering av medisinsk utstyr har mer informasjon om bla. anskaffelse, opplæring, vedlikehold og håndtering.
Oversikt over de ulike rollene for markedsdeltaker
| Markedsdeltaker | Definisjon i MDR artikkel 2 og IVDR artikkel 2 |
|---|---|
| Produsent | en fysisk eller juridisk person som framstiller eller helrenoverer utstyr, eller som får utstyr designet, framstilt eller helrenovert, og som markedsfører nevnte utstyr i eget navn eller under eget varemerke. |
| Autorisert representant | enhver fysisk eller juridisk person etablert i Unionen* som har fått og har akseptert en skriftlig fullmakt fra en produsent plassert utenfor Unionen, til å utføre bestemte oppgaver på dennes vegne med hensyn til dennes forpliktelser i henhold til denne forordning. |
| Importør | enhver fysisk eller juridisk person etablert i Unionen* som bringer utstyr fra en tredjestat i omsetning i Unionen*. |
| Distributør | enhver fysisk eller juridisk person i omsetningskjeden, utenom produsenten eller importøren, som gjør utstyr tilgjengelig på markedet fram til ibruktaking. |
| Helseinstitusjon | en organisasjon som har som hovedformål å pleie eller behandle pasienter eller fremme folkehelsen. |
* Med «Unionen» menes her EU/EØS-området og Tyrkia.
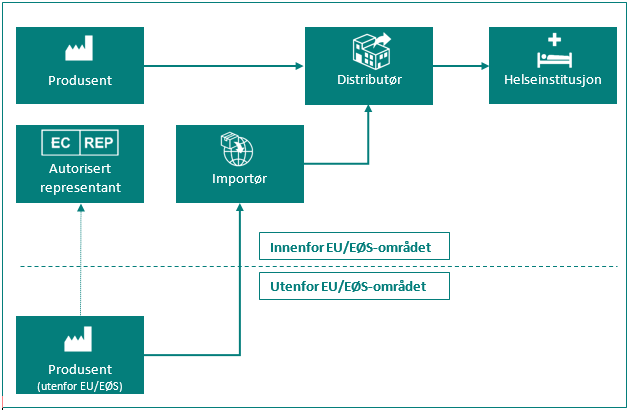
Figur: Markedsdeltaker i omsetningskjeden.